Mielofibrosis
Tipos de mielofibrosis
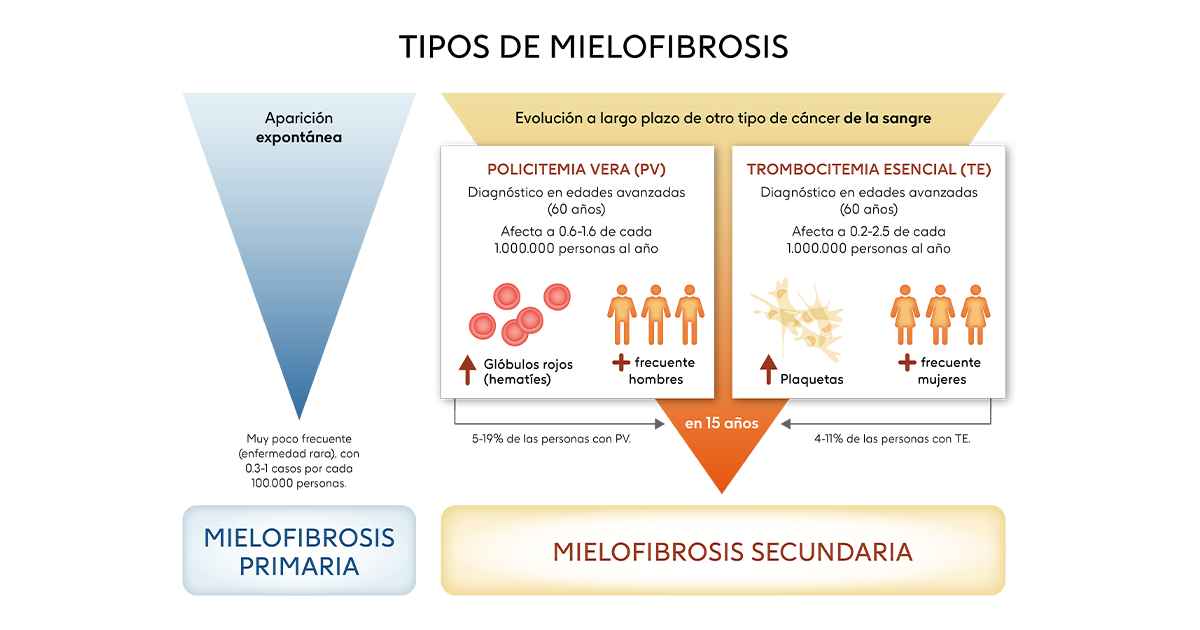
Hay dos tipos de mielofibrosis dependiendo de su origen, aunque esto no impacta en las características clínicas de la enfermedad, que son similares en los dos tipos [1]:
Causas de la mielofibrosis
Lo que provoca que la célula madre sanguínea sana se transforme en cancerígena es la adquisición de alteraciones (cambios denominados mutaciones) en la información contenida en el material genético (genes) de dicha célula [11]. Mayoritariamente son tres genes los que resultan afectados: JAK2, CALR y MPL. Con la información que contienen estos genes, en condiciones normales, el organismo fabrica diferentes proteínas que interaccionan con otras produciéndose una serie de reacciones en cadena. Esas reacciones hacen que se activen o desactiven otras proteínas (vía de señalización JAK/STAT) [12] que controlan que las células madre sanguíneas se dividan adecuadamente en la médula ósea y se produzcan las células de la sangre necesarias (hematíes, glóbulos blancos y plaquetas) [2].
Los genes JAK2, CALR y MPL se encuentran mutados en el 60%, 20-30% y 7-10% de los casos de mielofibrosis, respectivamente [13]. En la mayoría de los casos, las mutaciones en estos genes son las responsables de que se desarrolle la mielofibrosis, aunque hay pacientes con mielofibrosis en los que no se ha detectado mutaciones en ninguno de estos genes [14]. También se han descrito alteraciones en otros genes que, aunque no desencadenen la mielofibrosis, pueden contribuir al pronóstico de la misma (p. ej. ASXL1, SRSF2, U2AF1, EZH2, TET2, IDH1/2, SF3B1...) [2, 15-17].
Las proteínas que se generan a partir de los genes JAK2, CALR y MPL alterados no funcionan adecuadamente y no consiguen controlar la división de las células madre sanguíneas. Esto provoca que se pierda el equilibrio entre las células que se mueren y las nuevas que se generan (recambio celular) [18]. Las células madre sanguíneas alteradas se dividen descontroladamente y se acumulan en la medula ósea y producen sustancias que alteran a otras células de la médula ósea provocando, entre otros efectos, la fibrosis [5, 19].
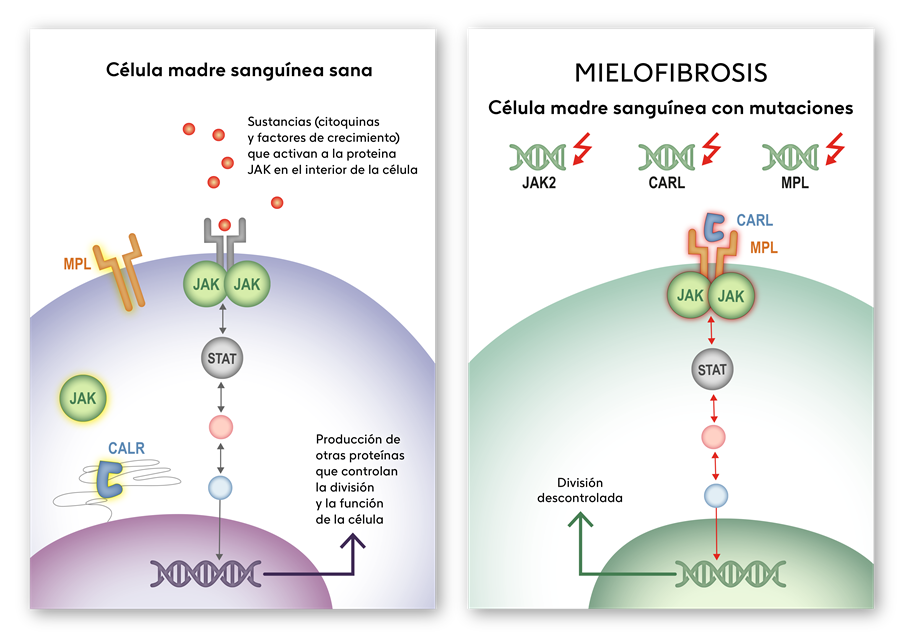
Figura 2. Señalización de los genes. (Figura creada por Lidesec para GSK)
Como consecuencia de todo ello se disminuye la producción de células sanguíneas (hematíes, glóbulos blancos y plaquetas) [20] en la médula ósea. Para intentar resolver esa situación, las células madre sanguíneas migran desde la médula ósea a otros lugares en los que puedan producir las células sanguíneas necesarias (p. ejemplo, bazo e hígado) [15, 19, 21, 22].
Factores de riesgo
Género.
Aunque la mielofibrosis primaria afecta por igual a hombres y mujeres [23], se ha observado que en los hombres puede evolucionar a mielofibrosis secundaria desde otras enfermedades como policitemia vera y trombocitemia esencial [24]. El género masculino es donde se detecta con mayor frecuencia una de las mutaciones más frecuentes del gen JAK2 [8, 25].
Edad avanzada.
El diagnóstico de mielofibrosis primaria suele realizarse en personas con edades comprendidas entre los 60 y 70 años; únicamente se diagnostica con 40 y 50 años en el 5% y 17% de los casos, respectivamente [26]. La edad es un factor de riesgo para que se produzcan mutaciones en los genes JAK2 [25].
Presencia de mutaciones hereditarias.
Generalmente la mielofibrosis primaria no es hereditaria, es decir, no se suele transmitir de padres a hijos. Sin embargo, se ha descrito que un tipo de mutación en el gen JAK2 puede ser heredada, constituyendo un factor de riesgo para desarrollar mielofibrosis primaria [25, 27].
Factores ambientales.
Se ha descrito en algunos casos de mielofibrosis la exposición previa a radiaciones ionizantes o a tóxicos industriales (benzeno o tolueno) [28, 29]. Por otra parte, el humo del tabaco también aumenta el riesgo de que aparezcan mutaciones en varios de los genes implicados en el desarrollo de mielofibrosis (JAK2 y CARL) [25, 30].
Trombocitemia esencial
Además, la evolución de policitemia vera (PV) y (TE) a mielofibrosis puede estar relacionada con otros factores como [9]: una larga duración de la enfermedad previa, la presencia de muchos síntomas y determinadas alteraciones genéticas
Desde GSK Oncohematología tenemos el compromiso de Transformar juntos el cáncer en Esperanza. Esto significa apoyar el conocimiento y prevención de la enfermedad, trabajando por una investigación, desarrollo e innovación continua, que ayude a cambiar la calidad de vida de los pacientes.
Referencias
- Masarova L, Bose P, Daver N, et al. Patients with post-essential thrombocythemia and post-polycythemia vera differ from patients with primary myelofibrosis. Leuk Res. 2017;59:110-6.
- Tefferi A. Primary myelofibrosis: 2023 update on diagnosis, risk-stratification, and management. Am J Hematol. 2023;98(5):801-21.
- Garrote M, López-Guerra M, Arellano-Rodrigo E, et al. Clinical Characteristics and Outcomes of Patients with Primary and Secondary Myelofibrosis According to the Genomic Classification Using Targeted Next-Generation Sequencing. Cancers (Basel). 2023;15(15):3904
- Verstovsek S, Yu J, Scherber RM, et al. Changes in the incidence and overall survival of patients with myeloproliferative neoplasms between 2002 and 2016 in the United States. Leuk Lymphoma. 2022;63(3):694-702.
- Arber DA, Orazi A, Hasserjian RP, et al. International Consensus Classification of Myeloid Neoplasms and Acute Leukemias: integrating morphologic, clinical, and genomic data. Blood. 2022;140(11):1200-28.
- Masarova L, Verstovsek S. The evolving understanding of prognosis in post-essential thrombocythemia myelofibrosis and post-polycythemia vera myelofibrosis vs primary myelofibrosis. Clin Adv Hematol Oncol. 2019;17(5):299-307.
- Thapa B, Fazal S, Parsi M, et. Al. Myeloprliferative Neoplasms. StatPearls Publishing; 2023.
- Greenfield G, McMullin MF, Mills K. Molecular pathogenesis of the myeloproliferative neoplasms. J Hematol Oncol. 2021;14(1):103.
- Lu X, Chang R. Polycythemia Vera. StatPearls Publishing; 2023
- Accurso V, Santoro M, Mancuso S, et al. The Essential Thrombocythemia in 2020: What We Know and Where We Still Have to Dig Deep. Clin Med Insights Blood Disord. 2020;13:2634853520978210.
- MedlinePlus. Primary myelofibrosis. [Internet]. 2014. [Último acceso: febrero 2024]. Disponible en: https://medlineplus.gov/genetics/condition/primary-myelofibrosis/#inheritance
- Staerk J, Constantinescu SN. The JAK-STAT pathway and hematopoietic stem cells from the JAK2 V617F perspective. Jakstat. 2012;1(3):184-90.
- Luque Paz D, Kralovics R, Skoda RC. Genetic basis and molecular profiling in myeloproliferative neoplasms. Blood. 2023;141(16):1909-21.
- Al-Ghamdi YA, Lake J, Bagg A, et al. Triple-Negative Primary Myelofibrosis: A Bone Marrow Pathology Group Study. Mod Pathol. 2023;36(3):100016.
- Mascarenhas J, Gleitz HFE, Chifotides HT, et al. Biological drivers of clinical phenotype in myelofibrosis. Leukemia. 2023;37(2):255-64.
- Rumi E, Trotti C, Vanni D, et al. The Genetic Basis of Primary Myelofibrosis and Its Clinical Relevance. Int J Mol Sci. 2020;21(23):885.
- Chifotides HT, Verstovsek S, Bose P. Association of Myelofibrosis Phenotypes with Clinical Manifestations, Molecular Profiles, and Treatments. Cancers (Basel). 2023;15(13):3331.
- Garmezy B, Schaefer JK, Mercer J, et al. A provider's guide to primary myelofibrosis: pathophysiology, diagnosis, and management. Blood Rev. 2021;45:100691.
- GAMFIN (Grupo Andaluz de Neoplasias Mieloproliferativas Crónicas Filadelfia negativa). Miniguía de la MIELOFIBROSIS. Recomendaciones básicas para el diagnóstico, pronóstico y tratamiento. [Internet]. 2015. [Último acceso: febrero de 2024]. Disponible en: https://www.sehh.es/publicaciones/guias-y-documentos/2981-mielofibrosis-recomendaciones-basicas-para-el-diagnostico-pronostico-y-tratamiento
- Passamonti F, Mora B. Myelofibrosis. Blood. 2023;141(16):1954-70.
- Yang X, Chen D, Long H, et al. The mechanisms of pathological extramedullary hematopoiesis in diseases. Cell Mol Life Sci. 2020;77(14):2723-38.
- Leukemia & Lymphoma Society. FS-14S Información sobre la mielofibrosis. [Internet]. [Ultimo acceso: febrero 2024]. Disponible en: https://www.lls.org/sites/default/files/file_assets/PS14S_Myelofibrosis_FactSheet_SPA10.12%20FINAL.pdf
- Orphanet. Primary myelofibrosis. [Internet]. 2019. [Último acceso: febrero 2024]. Disponible en: https://www.orpha.net/consor/cgi-bin/Disease_Search.phplng=EN&data_id=8745&Disease_Disease_Search_diseaseGroup=myelofibrosis&Disease_Disease_Search_diseaseType=Pat&Disease(s)/group%20of%20diseases=Primary-myelofibrosis&title=Primary%20myelofibrosis&search=Disease_Search_Simple
- Karantanos T, Chaturvedi S, Braunstein EM, et al. Sex determines the presentation and outcomes in MPN and is related to sex-specific differences in the mutational burden. Blood Adv. 2020;4(12):2567-76.
- Ramanathan G, Hoover BM, Fleischman AG. Impact of Host, Lifestyle and Environmental Factors in the Pathogenesis of MPN. Cancers (Basel). 2020;12(8):2038.
- Elkourashy S, Soliman D, Chandra P, et al. Primary Myelofibrosis in Young Patients ≤50 Years: Clinicopathological Characteristics, Genetic Landscape and Disease Outcome. A Single Center Experience. Hemasphere. 2022;23(6):1922-1923.
- Xia Y, Hong Q, Gao Z, et al. Somatically acquired mutations in primary myelofibrosis: A case report and meta-analysis. Exp Ther Med. 2021;21(3):193.
- GAMFIN: Grupo Andaluz de Neoplasias Mieloproliferativas Crónicas Filadelfia negativa. Manual para el manejo de pacientes con mielofibrosis. [Internet]. 2015 [Último acceso: febrero 2024] Disponible en: https://www.google.es/url?sa=i&rct=j&q=&esrc=s&source=web&cd=&cad=rja&uact=8&ved=0CDQQw7AJahcKEwjQiJuO1_eAAxUAAAAAHQAAAAAQAw&url=https%3A%2F%2Fwww.sehh.es%2Fimages%2Fstories%2Frecursos%2F2015%2Fnoticias%2FMANUAL_MF_GAMFIN.pdf&psig=AOvVaw2_IqLqkSSpUKjqbDHoDgET&ust=1693048450835023&opi=89978449
- Mughal TI, Vaddi K, Sarlis NJ, et al. Myelofibrosis-associated complications: pathogenesis, clinical manifestations, and effects on outcomes. Int J Gen Med. 2014;7:89-101.
- Allahverdi N, Yassin M, Ibrahim M. Environmental Factors, Lifestyle Risk Factors, and Host Characteristics Associated With Philadelphia Negative Myeloproliferative Neoplasm: A Systematic Review. Cancer Control. 2021;28:10732748211046802.
UA Marzo 2024: NP-ES-MML-PINS-230003(v1)
